در دنیای صنعتی امروز، تولید پسماندها و ضایعات اسیدی یکی از چالشهای بزرگ زیست محیطی و بهداشتی است. از کارخانههای فلزکاری تا صنایع پتروشیمی، هر جایی که فرآیندهای شیمیایی انجام میشود، احتمال تولید اسیدهای زائد وجود دارد. اگر این پسماندها به صورت اصولی مدیریت نشوند، میتوانند خاک، آب و هوا را آلوده کرده و سلامت انسان و محیط زیست را به خطر بیندازند.
در این مقاله با روشهای نوین، قانونی و ایمن برای امحا و بازیافت پسماندهای اسیدی آشنا میشویم و بررسی میکنیم چگونه میتوان با کمترین هزینه و بیشترین بازده، این مواد خطرناک را به منابع ارزشمند تبدیل کرد.
فهرست مطالب
- پسماند اسیدی چیست؟
- منابع تولید پسماندها و ضایعات اسیدی
- خطرات زیستمحیطی و انسانی پسماندهای اسیدی
- روشهای نوین امحا پسماندهای اسیدی
- بازیافت پسماندهای اسیدی و استفاده مجدد
- قوانین و الزامات قانونی در ایران
- جدول مقایسه روشهای امحا و بازیافت اسید
- جمعبندی
- سؤالات متداول
پسماند اسیدی چیست؟
پسماند اسیدی به هر نوع ماده زائدی گفته میشود که دارای خاصیت اسیدی (pH کمتر از 7) بوده و در اثر فرآیندهای صنعتی، شیمیایی یا حتی آزمایشگاهی تولید میشود.
این پسماندها ممکن است شامل اسید سولفوریک، اسید نیتریک، اسید کلریدریک یا ترکیبات اسیدی فلزی باشند.
مثال: در صنعت آبکاری فلزات، محلولهای اسیدی پس از مدتی خاصیت خود را از دست داده و به صورت پسماند اسیدی دور ریخته میشوند.
منابع تولید پسماندها و ضایعات اسیدی
در جدول زیر مهمترین منابع تولیدکننده پسماند اسیدی را مشاهده میکنید:
|
صنعت یا فعالیت |
نوع اسید مصرفی/تولیدی |
نمونه پسماند اسیدی |
| صنایع فلزکاری | اسید سولفوریک، نیتریک | محلولهای شستوشوی فلزات |
| صنایع باتریسازی | اسید سولفوریک | مایع باتریهای مستعمل |
| صنایع نساجی و رنگرزی | اسید فرمیک، استیک | پسابهای رنگی و اسیدی |
| صنایع پتروشیمی | اسید کلریدریک | پسابهای فرآیندهای شیمیایی |
| آزمایشگاهها | ترکیبات مختلف اسیدی | محلولهای تست و شستوشو |
خطرات زیستمحیطی و انسانی پسماندهای اسیدی
پسماندهای اسیدی اگر بدون تصفیه دفع شوند، اثرات مخربی دارند:
تأثیر بر محیط زیست
- آلودگی خاک: کاهش pH خاک و نابودی باکتریهای مفید.
- آلودگی آبهای زیرزمینی: نفوذ اسید به سفرههای آب و تغییر ترکیب شیمیایی آن.
- آلودگی هوا: در اثر تبخیر یا واکنش با دیگر مواد شیمیایی.
تأثیر بر سلامت انسان
- سوختگیهای شیمیایی پوست و چشم
- مشکلات تنفسی ناشی از بخارات اسیدی
- اختلال در عملکرد سیستم عصبی در مواجهه طولانیمدت
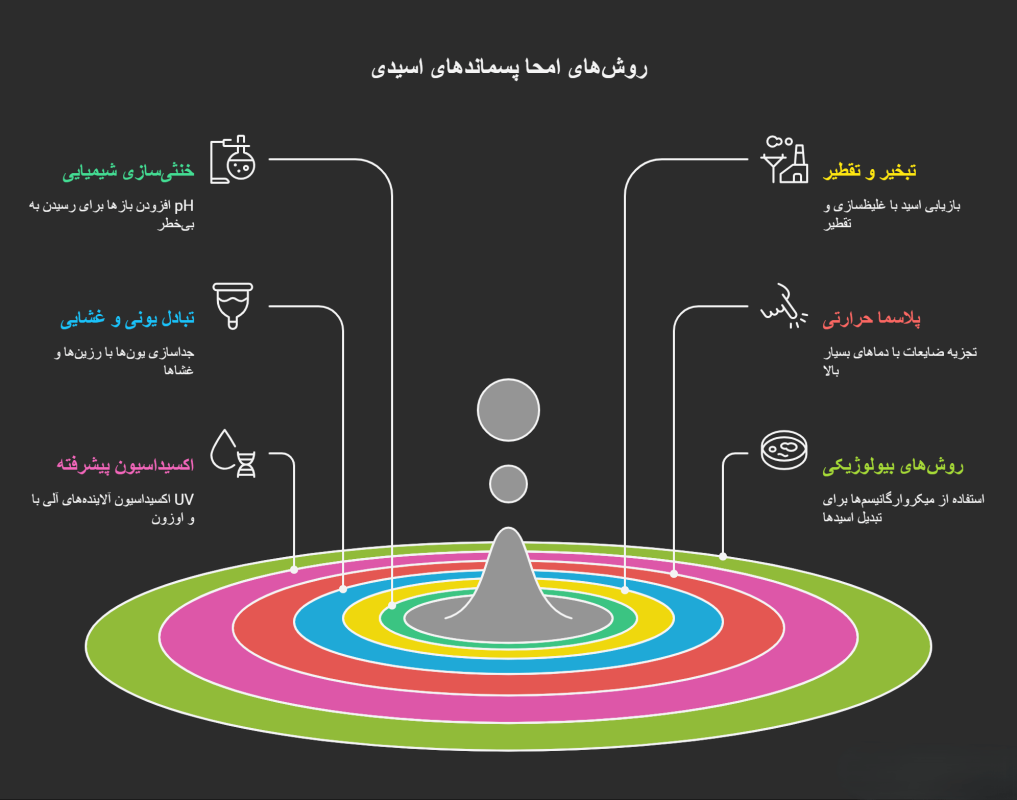
روشهای نوین امحا پسماندهای اسیدی
انتخاب روش امحا یا بازیافت پسماند اسیدی بستگی دارد به:
- نوع اسید (سولفوریک، کلریدریک، نیتریک و…),
- غلظت و حجم پسماند،
- ناخالصیها (فلزات سنگین، آلیاژها، محلولهای ارگانیک)،
- هدف: امحا کامل یا بازیافت،
- محدودیتهای محیط زیستی و اقتصادی.
در عمل ترکیبی از روشها (مثلاً خنثیسازی + تصفیه بعدی؛ یا تبخیر + تقطیر) معمول است.
1) خنثیسازی شیمیایی (Chemical neutralization)
اصول و واکنشها
- اساس: افزودن باز (آهک هیدراته Ca(OH)₂ یا سود NaOH) به اسید تا pH به محدوده بیخطر (معمولاً 6.5–8.5) برسد.
- مثال واکنش برای اسید سولفوریک:
H2SO4 + Ca(OH)2 → CaSO4 ↓ + 2 H2O
تجهیزات و روند عملی
- مخازن همزن (stirred tanks) با سیستم تزریق باز و کنترل pH اتوماتیک.
- پمپهای باز یا آهک به صورت سوسپانسیون.
- سیستم تهنشینی و فیلترپرس برای جداسازی لجن (ژیپس یا سولفات کلسیم).
پارامترهای کنترلی
- هدف pH: 6.5–8.0 (بسته به استاندارد محلی).
- نرخ افزودن باز: تا زمانی که کنترل pH بهصورت نرمافزاری انجام شود.
- دمای فرآیند: معمولی (خنثیسازی غالباً در دمای محیط).
مزایا/معایب
- مزایا: ارزان، ساده، قابل اجرا در حجم متوسط.
- معایب: تولید لجن (حجم و نیاز به دفع)، احتمال نمکزدایی ناقص.
نکات کاربردی و ایمنی
- همیشه افزودن اسید به آب (نه عکس) — اما در عمل پسماند اسیدی را در مخزن رقیق و سپس باز را اضافه کنید.
- کنترل دما برای جلوگیری از افزایش ناگهانی دما در واکنشهای قوی.
- PPE: شیلد صورت، دستکش مقاوم شیمیایی، لباس ضدپاشش.
مثال عددی (استوکیومتری) — خنثیسازی H₂SO₄ با Ca(OH)₂
ماحصل: 1 مول H₂SO₄ با 1 مول Ca(OH)₂ واکنش میدهد.
- جرم مولی H₂SO₄ = 98.079 g/mol.
- جرم مولی Ca(OH)₂ = 74.093 g/mol.
اگر 98.079 گرم H₂SO₄ داشته باشیم، برای خنثی نیاز به 74.093 گرم Ca(OH)₂ است.
(محاسبات: 98.079 ÷ 98.079 = 1 مول → نیاز 1 مول Ca(OH)₂ → 1 × 74.093 = 74.093 g)
2) تبخیر، تقطیر و بازیابی اسید (Evaporation & Distillation recovery)
چه زمانی مناسب است؟
وقتی اسید با خلوص اقتصادی قابل بازیافت باشد (مثلاً اسید سولفوریک یا کلریدریک با مقدار قابل توجه).
روند و تجهیزات
- برجهای تبخیر یا اواپراتورهای صنعتی (حرارتی یا با خلأ) برای غلیظسازی.
- مبدلهای حرارتی، کندانسورها و ستونهای تقطیر برای بازیابی اسید خالص.
- واحد کنترل ناخالصی و نیتریفیکاسیون در صورت نیاز.
پارامترهای عملیاتی
- خلأ برای کاهش نقطه جوش و صرفهجویی انرژی.
- کنترل جریان و بازده تقطیر (درصد بازیابی).
مزایا/معایب
- مزایا: بازگشت اسید به چرخه تولید، کاهش هزینه خرید مواد شیمیایی.
- معایب: سرمایه اولیه بالا، نیاز به مصرف انرژی و نگهداری.
3) تبادل یونی و روشهای غشایی (Ion-exchange, Electrodialysis, RO)
تبادل یونی
- از رزینهای کاتیونی/آنیونی برای گرفتن یونهای اسیدی یا ناخالصیها استفاده میشود.
- مناسب برای خالصسازی محلولهای با حجم کم/متوسط مثل پسابهای آزمایشگاهی یا خطوط صنعتی خاص.
الکترودیالیز (Electrodialysis)
- برای جداسازی یونها با استفاده از میدان الکتریکی و غشاهای یونی.
- مصرف برق دارد ولی برای بازیابی اسیدهای معدنی در مقیاس بالا کاربردی است.
اسمز معکوس (RO) + نانوفیلتراسیون
- غشاها یونهای کوچک را جدا میکنند؛ برای غلیظسازی محلول اسیدی و حذف ناخالصیها کاربرد دارد.
- حساس به رسوب و نیازمند پیشتصفیه.
4) پلاسما حرارتی و سوزاندههای پیشرفته (Thermal plasma, High-temp incineration)
کاربردها
- برای ضایعات پیچیده و مخلوطهای خطرناک که قابل خنثیسازی یا بازیافت مستقیم نیستند.
- دماهای بسیار بالا (هزاران درجه) که مولکولها را تجزیه میکنند و بدنهای از گازهای ساده و مولکولهای بیخطر میسازند.
نکات
- سرمایه و انرژی بالا؛ مناسب برای ضایعات با ارزش پایین اما خطر بالا.
- خروجی گازها باید تصفیه و پایش دقیق داشته باشد.
5) روشهای پیشرفته اکسیداسیون و بیولوژیکی (AOPs & Bio-neutralization)
اکسیداسیون پیشرفته (AOP)
- کاربرد بیشتر برای پسماندهای اسیدی همراه با آلودگی آلی (مثلاً اسیدهای ارگانیک یا حلالها).
- استفاده از ترکیبهای H₂O₂، UV، یا اوزون برای اکسیداسیون کامل آلایندههای آلی.
بیولوژیکی
- استفاده از میکروارگانیسمهای خاص که اسیدها یا ترکیبات زیانآور را مصرف/تبدیل میکنند.
- مزیت: پایدار و کمهزینه در بلندمدت؛ معایب: حساس به pH بسیار پایین و ناخالصیهای سمی.
6) مدیریت لجن و پسابهای جانبی
- پس از خنثیسازی، لجن باید تهنشین، آبگیری (فیلترپرس/سانتریفیوژ) و نمونهبرداری برای فلزات سنگین شود.
- امکان استفاده مجدد لجن (مثلاً سولفات کلسیم در سیمان یا مصالح ساختمانی) در صورتی که استانداردهای فلزی را پاس کند.
جدول خلاصه فنی (پارامترها و کاربردها)
|
روش |
دوره سرمایهای | هزینه عملیاتی | پسماند ثانویه |
کاربرد توصیهای |
| خنثیسازی شیمیایی | کم | کم | لجن (ژیپس/نمک) | صنایع کوچک/متوسط |
| تبخیر/تقطیر | زیاد | متوسط-زیاد | ناخالصیهای تغلیظشده | صنایع بزرگ، بازیافت اسید |
| تبادل یونی | متوسط | متوسط | رزین اشباع | خالصسازی محلولها |
| الکترودیالیز/رو | زیاد | متوسط | محلول غلیظ | بازیافت و غلیظسازی اسید |
| پلاسما حرارتی | بسیار زیاد | زیاد | گازهای قابل تصفیه | ضایعات خطرناک مختلط |
| بیولوژیکی/AOP | متوسط | کم-متوسط | زیستی یا CO₂ آب | آلایندههای آلی همراه اسید |
نکات عملی برای پیادهسازی در کارخانه یا واحد صنعتی
- نمونهبرداری و آنالیز: همیشه قبل از انتخاب روش، آنالیز کامل pH، هدایتالکتریکی، فلزات سنگین، TOC و ترکیبات آلی انجام دهید.
- پایلوت و تست: قبل از راهاندازی مقیاس کامل از واحد پایلوت استفاده کنید.
- پایش مداوم: حسگر pH آنلاین، TOC متر و اندازهگیری یونها ضروریاند.
- ایمنی و آموزش کارکنان: دستورالعملهای SOP، ارزیابی ریسک و PPE.
- ثبت و مستندسازی براى تطابق قانونی: نگهداری گزارشهای تحویل پسماند و نتایج آزمایشات طبق مقررات محیطزیست.
برای امحا یا بازیافت پسماندهای اسیدی راهکار واحدی وجود ندارد؛ انتخاب به نوع اسید، حجم، ناخالصی و هدف اقتصادی بستگی دارد. در عمل، ترکیبی از خنثیسازی، بازیابی (تقطیر/تبخیر) و روشهای غشایی یا پلاسما بسته به شرایط بهترین نتیجه را میدهد. تمرکز باید روی کاهش تولید لجن، بازیابی و بازچرخانی و پایش دقیق پارامترهای کلیدی باشد.
اگر دوست دارید، میتوانم:
- یک SOP (دستورالعمل عملیاتی استاندارد) برای خنثیسازی و مدیریت لجن (قابل چاپ) آماده کنم، یا
- یک چکلیست پایلوت برای تست قابلیت بازیافت اسید در کارخانه شما بنویسم.
بازیافت پسماندهای اسیدی و استفاده مجدد
بازیافت اسیدها نهتنها از آلودگی جلوگیری میکند، بلکه باعث صرفهجویی اقتصادی قابل توجهی نیز میشود.
مهمترین روشهای بازیافت:
- بازیافت فیزیکی: جداسازی اسید از ناخالصیها با تبخیر یا فیلتر.
- بازیافت شیمیایی: احیای ترکیبات اسیدی به مواد اولیه قابل استفاده.
- بازیافت فلزات از اسیدها: استخراج فلزاتی مانند مس، روی و نیکل از محلولهای اسیدی.
نمونه موردی:
در صنعت باتری، اسید سولفوریک باتریهای فرسوده بهجای تخلیه در طبیعت، با فرآیند خنثیسازی و تصفیه، مجدداً در تولید باتریهای جدید استفاده میشود.
قوانین و الزامات قانونی در ایران
مدیریت پسماندهای خطرناک از جمله پسماندهای اسیدی در ایران طبق قانون مدیریت پسماندها (مصوب ۱۳۸۳) و آییننامه اجرایی آن، الزامی است.
مهمترین نکات قانونی:
- هر تولیدکننده موظف است پسماند اسیدی خود را تا زمان تحویل به مراکز مجاز، بهصورت ایمن ذخیرهسازی کند.
- انتقال، حمل و دفن پسماندهای اسیدی تنها با مجوز سازمان حفاظت محیط زیست مجاز است.
- شرکتهای دارای مجوز مانند واحدهای “تصفیه و امحای پسماند شیمیایی” میتوانند عملیات بازیافت یا امحا را انجام دهند.
جدول مقایسه روشهای امحا و بازیافت اسید
|
روش |
نوع فرآیند | مزایا | معایب |
کاربرد اصلی |
| خنثیسازی شیمیایی | شیمیایی | ساده و ارزان | تولید لجن | صنایع کوچک و متوسط |
| تبخیر و بازیافت | فیزیکی | بازیافت اسید | نیاز به انرژی بالا | صنایع بزرگ |
| تبادل یونی | شیمیایی | دقت بالا | هزینه رزین بالا | آزمایشگاهها |
| پلاسما حرارتی | فیزیکی/حرارتی | بدون آلودگی | هزینه بالا | ضایعات خطرناک |
| بیولوژیکی | زیستی | پایدار و سبز | در حال توسعه | صنایع جدید سبز |
جمعبندی
پسماندها و ضایعات اسیدی، اگرچه خطرناکاند، اما با مدیریت صحیح و استفاده از روشهای نوین و قانونی امحا و بازیافت میتوانند به منابعی سودآور تبدیل شوند.
امروزه شرکتها با استفاده از فناوریهایی مانند تبخیر، تبادل یونی و پلاسما نهتنها محیط زیست را حفظ میکنند، بلکه هزینههای تولید خود را نیز کاهش میدهند.
بهطور خلاصه، آینده صنایع در گرو بازیافت سبز و مدیریت هوشمند پسماندهای شیمیایی است.
سؤالات متداول بازیافت پسماندهای اسیدی
-
پسماند اسیدی چیست؟
پسماند اسیدی هر ماده زائدی است که دارای خاصیت اسیدی باشد و از فرآیندهای صنعتی یا آزمایشگاهی بهدست آید.
-
آیا میتوان پسماندهای اسیدی را به فاضلاب ریخت؟
خیر. تخلیه مستقیم اسید به فاضلاب غیرقانونی و بسیار خطرناک است. باید ابتدا خنثیسازی انجام شود.
-
بهترین روش امحا پسماند اسیدی چیست؟
برای صنایع کوچک، خنثیسازی شیمیایی و برای صنایع بزرگ، بازیافت با تبخیر یا پلاسما مناسبتر است.
-
چه قوانینی در ایران برای پسماندهای اسیدی وجود دارد؟
قانون مدیریت پسماندها و آییننامه اجرایی آن که تحت نظارت سازمان حفاظت محیط زیست اجرا میشود.
-
آیا بازیافت پسماند اسیدی صرفه اقتصادی دارد؟
بله، زیرا از اسیدها و فلزات قابلاستخراج مجدداً در تولید استفاده میشود و هزینه خرید مواد اولیه کاهش مییابد.

