اسید سولفوریک (Sulfuric Acid) یکی از پرکاربردترین و مهمترین اسیدهای معدنی در جهان است. از تولید کود شیمیایی و باتری گرفته تا صنایع دارویی، نفتی و فلزکاری، ردپای این مادهی بیهمتا را میتوان در همه جا دید. اما دقیقاً اسید سولفوریک چیست، چگونه تولید میشود و چه کاربردهایی دارد؟ در این مقاله به زبان ساده و کاربردی همه چیز را توضیح میدهیم.
فهرست مطالب
- اسید سولفوریک چیست؟
- فرمول شیمیایی و ساختار مولکولی اسید سولفوریک
- ویژگیهای فیزیکی و شیمیایی اسید سولفوریک
- روشهای تولید اسید سولفوریک
- کاربردهای اسید سولفوریک در صنایع مختلف
- نکات ایمنی هنگام کار با اسید سولفوریک
- جمعبندی: چرا شناخت اسید سولفوریک اهمیت دارد؟
اسید سولفوریک چیست؟
اسید سولفوریک با فرمول شیمیایی H₂SO₄ یک اسید معدنی بسیار قوی و خورنده است که از ترکیب گوگرد، اکسیژن و هیدروژن بهدست میآید. این ماده بیرنگ، چگال و روغنیشکل است و با آب واکنش شدیدی میدهد.
بهطور کلی، اسید سولفوریک یکی از مهمترین محصولات صنایع شیمیایی بهشمار میرود. حتی در بسیاری از کشورها، میزان تولید سالانه اسید سولفوریک را بهعنوان شاخص توسعه صنعتی در نظر میگیرند.
فرمول شیمیایی و ساختار مولکولی
فرمول شیمیایی اسید سولفوریک به صورت H₂SO₄ نوشته میشود. در این ترکیب:
- دو اتم هیدروژن (H)،
- یک اتم گوگرد (S) و
- چهار اتم اکسیژن (O) وجود دارند.
ساختار مولکولی آن شامل یک اتم مرکزی گوگرد است که با چهار اکسیژن پیوند دارد. دو تا از این اکسیژنها با هیدروژن ترکیب شدهاند و خاصیت اسیدی ماده را ایجاد میکنند. این ترکیب باعث میشود که اسید سولفوریک، یک اسید دوپروتونی قوی باشد.
ویژگیهای فیزیکی و شیمیایی اسید سولفوریک
ویژگیهای فیزیکی
- رنگ: بیرنگ تا زرد کمرنگ
- بو: بیبو (اما در واکنش با مواد دیگر میتواند بخارات سمی تولید کند)
- حالت: مایع غلیظ و روغنی شکل
- چگالی: حدود 1.84 گرم بر سانتیمتر مکعب
- نقطه جوش: 337 درجه سانتیگراد
- نقطه ذوب: 10 درجه سانتیگراد
ویژگیهای شیمیایی
اسید سولفوریک خاصیت خورندگی و آبگیری بسیار قوی دارد. این اسید میتواند با بیشتر فلزات، بازها، آب و حتی مواد آلی واکنش دهد. از جمله مهمترین واکنشهای آن میتوان به موارد زیر اشاره کرد:
- واکنش با فلزات برای تولید هیدروژن
- واکنش با بازها برای تشکیل نمک و آب
- تجزیه مواد آلی به دلیل خاصیت دهیدراتهکنندگی بالا
روشهای تولید اسید سولفوریک
تولید صنعتی اسید سولفوریک یکی از فرآیندهای مهم و استراتژیک در صنایع شیمیایی محسوب میشود. این اسید از منابع مختلفی نظیر گوگرد عنصری، سولفیدهای فلزی، گاز طبیعی و حتی گازهای حاصل از فرایندهای صنعتی تولید میشود. در حال حاضر دو روش اصلی برای تولید اسید سولفوریک وجود دارد که عبارتند از فرآیند تماسی (Contact Process) و فرآیند اتاق سربی (Lead Chamber Process). در ادامه هر یک را به تفصیل بررسی میکنیم.
1. فرآیند تماسی (Contact Process)
فرآیند تماسی پیشرفتهترین و پرکاربردترین روش تولید اسید سولفوریک در جهان است و حدود ۹۵٪ تولید جهانی از این طریق انجام میشود. این فرآیند شامل چند مرحله کلیدی است:
- مرحله ۱: تولید گاز دیاکسید گوگرد (SO₂)
در این مرحله، گوگرد عنصری یا سولفیدهای فلزی مانند پیریت (FeS₂) در حضور اکسیژن سوزانده میشوند تا گاز SO₂ تولید شود:
S + O₂ → SO₂2FeS₂ + 5.5O₂ → Fe₂O₃ + 4SO₂
- مرحله ۲: خالصسازی گاز SO₂
گاز حاصل از احتراق دارای ناخالصیهایی مانند گرد و غبار، اکسیدهای فلزی و بخار آب است. برای جلوگیری از مسدود شدن کاتالیزور، این گاز در چند مرحله شامل شستوشو، خشکسازی و فیلتر کردن تصفیه میشود.
- مرحله ۳: اکسیداسیون گاز SO₂ به SO₃
گاز SO₂ تمیز سپس وارد برج کاتالیزوری میشود و در حضور کاتالیزور وانادیوم پنتااکسید (V₂O₅) در دمای حدود ۴۵۰ درجه سانتیگراد و فشار معمولی به تریاکسید گوگرد (SO₃) تبدیل میگردد:
2SO₂ + O₂ ⇌ 2SO₃ (ΔH = -197 kJ/mol)
این واکنش گرمازا و برگشتپذیر است، بنابراین کنترل دقیق دما و فشار اهمیت زیادی دارد.
- مرحله ۴: جذب SO₃ در اسید سولفوریک غلیظ
از آنجا که واکنش مستقیم SO₃ با آب بسیار شدید و خطرناک است، ابتدا آن را در اسید سولفوریک غلیظ جذب میکنند تا اولئوم (Oleum) یا “اسید دودزا” تولید شود:
SO₃ + H₂SO₄ → H₂S₂O₇
- مرحله ۵: رقیقسازی اولئوم
در آخر، اولئوم با مقدار مشخصی آب ترکیب میشود تا اسید سولفوریک با غلظت دلخواه (معمولاً ۹۸٪) تولید گردد:
H₂S₂O₇ + H₂O → 2H₂SO₄
✅ مزایای فرآیند تماسی:
- بازده بالا (تا ۹۸٪)
- تولید اسید با خلوص زیاد
- قابل کنترل بودن واکنشها
- امکان بازیافت حرارت و صرفهجویی در انرژی
⚠️ معایب:
- نیاز به تجهیزات مقاوم در برابر حرارت و خوردگی
- هزینه سرمایهگذاری اولیه بالا
۲. فرآیند اتاق سربی (Lead Chamber Process)
این روش از قرن نوزدهم برای تولید اسید سولفوریک استفاده میشد و امروزه کاربرد محدودی دارد. در این فرآیند، دیاکسید گوگرد (SO₂) در حضور بخار آب و اکسید نیتروژنها (NO و NO₂) در اتاقهایی از جنس سرب به اسید سولفوریک رقیق تبدیل میشود.
واکنشهای اصلی در فرآیند اتاق سربی:
SO₂ + NO₂ + H₂O → H₂SO₄ + NO2NO + O₂ → 2NO₂
در اینجا، گاز NO مجدداً به NO₂ اکسید میشود و در چرخه واکنش باقی میماند.
✅ مزایا:
- مناسب برای تولید اسید با غلظت پایین (۶۵ تا ۷۸ درصد)
- هزینه کمتر نسبت به فرآیند تماسی
⚠️ معایب:
- اسید تولیدی خلوص پایینی دارد
- کنترل واکنشها دشوارتر است
- به دلیل استفاده از اتاقهای سربی، خطر آلودگی زیستمحیطی بالاست
۳. روشهای جدید و بازیافتی
علاوه بر دو روش کلاسیک فوق، امروزه روشهای نوینی نیز برای تولید یا بازیافت اسید سولفوریک از ضایعات صنعتی توسعه یافتهاند:
- بازیافت از گازهای خروجی پالایشگاهها و صنایع فلزی (مانند تولید مس و روی)
- استفاده از اسیدهای spent acid (اسیدهای مصرفشده در فرایندهای نفتی) از طریق احیا و تقطیر
- فرآیندهای زیستمحیطی نوین برای کاهش انتشار SO₂ در هوا
این روشها نه تنها به صرفهجویی اقتصادی کمک میکنند، بلکه نقش مهمی در کاهش آلودگی هوا و کنترل انتشار گازهای گوگردی دارند.
فرآیند تماسی امروزه بهعنوان استاندارد جهانی تولید اسید سولفوریک شناخته میشود. این روش بازده بالا، خلوص زیاد و کنترل دقیق واکنشها را ممکن میسازد. با این حال، در کنار توسعه فناوریهای جدید و بازیافتی، آینده تولید این اسید به سمت روشهای پاکتر و پایدارتر حرکت میکند.

کاربردهای اسید سولفوریک
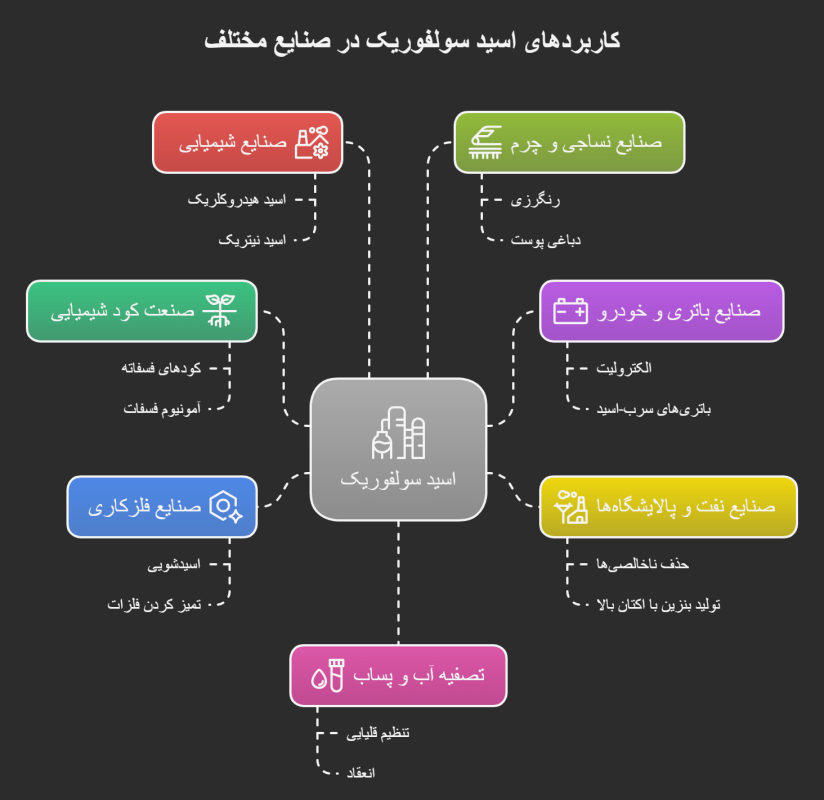
اسید سولفوریک به دلیل قدرت بالا و قیمت نسبتاً مناسب، در طیف وسیعی از صنایع استفاده میشود. در ادامه مهمترین کاربردهای آن را بررسی میکنیم:
- صنعت کود شیمیایی
بیش از ۶۰ درصد اسید سولفوریک تولیدی جهان در ساخت کودهای فسفاته مانند سوپر فسفاتها و آمونیوم فسفات به کار میرود. این کودها برای رشد بهتر گیاهان حیاتیاند.
- صنایع باتری و خودرو
اسید سولفوریک ماده اصلی الکترولیت در باتریهای سرب-اسید است که در خودروها استفاده میشود. این اسید جریان الکتریکی را بین صفحات سربی برقرار میکند و انرژی لازم برای استارت خودرو را فراهم میسازد.
- صنایع نفت و پالایشگاهها
در پالایش نفت خام، از اسید سولفوریک برای:
- حذف ناخالصیها،
- تولید بنزین با اکتان بالا،
- و تصفیه فرآوردههای نفتی استفاده میشود.
- صنایع فلزکاری
در فرآیند اسیدشویی (Pickling) برای تمیز کردن سطح فلزات مانند آهن و فولاد از زنگ و اکسیدها از اسید سولفوریک استفاده میشود. این مرحله پیش از آبکاری یا رنگکاری انجام میگیرد.
- صنایع شیمیایی
از اسید سولفوریک برای تولید مواد شیمیایی دیگر مانند:
- اسید هیدروکلریک
- اسید نیتریک
- سولفاتها
- رنگها و داروها استفاده میشود.
- صنایع نساجی و چرم
در رنگرزی، تولید الیاف مصنوعی، دباغی پوست و تصفیه آب از اسید سولفوریک برای تنظیم pH و حذف ناخالصیها بهره میگیرند.
- تصفیه آب و پساب
در تصفیهخانهها از اسید سولفوریک برای تنظیم میزان قلیائیت آب و کمک به فرایند انعقاد استفاده میشود.
نکات ایمنی هنگام کار با اسید سولفوریک
با وجود کاربردهای فراوان، اسید سولفوریک مادهای بسیار خطرناک و خورنده است و باید با دقت کامل استفاده شود. در ادامه مهمترین نکات ایمنی را مرور میکنیم:
✅ نکات مهم
- همیشه هنگام کار از دستکش مقاوم، عینک ایمنی و لباس مخصوص استفاده کنید.
- هرگز آب را به اسید اضافه نکنید! همیشه اسید را به آرامی به آب اضافه کنید.
- از تماس مستقیم با پوست و چشمها جلوگیری کنید.
- در محیطهای بسته از سیستم تهویه مناسب استفاده کنید.
- در صورت تماس با پوست، فوراً محل را با آب فراوان بشویید.
🚫 موارد ممنوع
- ذخیرهسازی در ظروف فلزی معمولی (چون باعث خوردگی میشود)
- مخلوط کردن با مواد آلی یا قلیایی بدون کنترل
- استفاده بدون تهویه در محیطهای بسته
اسید سولفوریک در محیط زیست
اسید سولفوریک یکی از خطرناکترین و در عین حال پرمصرفترین مواد شیمیایی در صنایع مختلف است. با وجود کاربردهای گسترده، اثرات زیستمحیطی آن میتواند در صورت عدم کنترل، بسیار مخرب باشد. این ماده در صورت نشت یا انتشار به محیط، بر آب، خاک، هوا و حتی سلامت انسان تأثیرات قابل توجهی دارد. در ادامه، جنبههای مختلف تأثیر اسید سولفوریک بر محیط زیست را بهصورت کامل بررسی میکنیم.
۱. تأثیر بر منابع آبی
وقتی اسید سولفوریک وارد منابع آب سطحی یا زیرزمینی میشود، باعث کاهش شدید pH آب و افزایش اسیدیته آن میگردد. این موضوع میتواند:
- تعادل اکولوژیکی رودخانهها و دریاچهها را بر هم بزند،
- باعث مرگ آبزیان حساس به تغییر pH شود،
- و فلزات سنگین مانند سرب و کادمیوم را از رسوبات آزاد کرده و وارد زنجیره غذایی کند.
نتیجه این فرآیند، آلودگی گسترده منابع آبی و تهدید سلامت انسان و حیوان است.
۲. تأثیر بر خاک
نشت یا بارش اسید سولفوریک میتواند خاک را اسیدی کند و عناصر ضروری آن مانند کلسیم، پتاسیم و منیزیم را از بین ببرد. در نتیجه:
- حاصلخیزی زمینهای کشاورزی کاهش مییابد،
- رشد گیاهان کند یا متوقف میشود،
- و باکتریهای مفید خاک از بین میروند.
در مناطق صنعتی که ذخیرهسازی یا حملونقل این اسید انجام میشود، معمولاً پوشش گیاهی از بین میرود و بازسازی خاک سالها زمان میبرد.
۳. تأثیر بر هوا و باران اسیدی
گاز دیاکسید گوگرد (SO₂) حاصل از فرآیندهای صنعتی در جو با بخار آب ترکیب شده و به اسید سولفوریک تبدیل میشود. این واکنش باعث شکلگیری باران اسیدی میگردد:
SO₂ + H₂O + ½O₂ → H₂SO₄
باران اسیدی موجب:
- فرسایش ساختمانها و آثار تاریخی،
- آسیب به برگ درختان و کاهش رشد گیاهان،
- و آلودگی آبهای سطحی میشود.
۴. خطرات برای انسان و حیوانات
تماس مستقیم با اسید سولفوریک یا بخارات آن میتواند منجر به سوختگی پوست، تحریک مجاری تنفسی و آسیب دائمی به چشمها شود. استنشاق مداوم بخارات این ماده در محیطهای صنعتی باعث بیماریهای مزمن ریوی میشود. حیوانات نیز از طریق نوشیدن آب آلوده یا تغذیه از گیاهان آلوده در معرض خطر قرار میگیرند.
۵. مدیریت و کاهش اثرات زیستمحیطی
برای جلوگیری از آلودگی محیط زیست توسط اسید سولفوریک، اقدامات پیشگیرانه و اصلاحی زیر ضروری است:
اقدامات پیشگیرانه:
- استفاده از مخازن مقاوم در برابر خوردگی برای ذخیره و حمل اسید.
- پایش مداوم نشت و بخارات در محلهای صنعتی.
- آموزش کارکنان برای واکنش سریع در شرایط اضطراری.
اقدامات اصلاحی:
- خنثیسازی اسید نشتکرده با مواد قلیایی مانند آهک یا سدیم بیکربنات.
- استفاده از سیستمهای تصفیه گاز (Scrubber) برای حذف SO₂ از دودکشها.
- بازیافت اسیدهای مصرفشده در صنایع نفتی و فلزی.
۶. فناوریهای نوین و تولید پایدار
در سالهای اخیر، صنایع شیمیایی به سمت تولید پایدار و سبز اسید سولفوریک حرکت کردهاند. از جمله:
- استفاده از فرآیندهای بسته برای جلوگیری از انتشار گازهای گوگردی،
- بازیافت حرارت حاصل از واکنشها برای صرفهجویی در انرژی،
- و توسعه فناوریهای کاهشدهنده انتشار دیاکسید گوگرد.
اسید سولفوریک با وجود اهمیت صنعتی بالا، در صورت رهاسازی یا نشت کنترلنشده، میتواند خسارتهای جبرانناپذیری بر محیط زیست وارد کند. مدیریت صحیح، فناوریهای پاک و نظارت دقیق، سه رکن اصلی کاهش اثرات زیستمحیطی این ماده هستند. با اتخاذ رویکردهای پایدار میتوان میان توسعه صنعتی و حفظ محیط زیست تعادل برقرار کرد.
جمعبندی
اسید سولفوریک یکی از پایههای اصلی صنایع مدرن است. از تولید کود شیمیایی و باتری خودرو گرفته تا پالایش نفت و ساخت دارو، همه به نوعی به این ماده وابستهاند.
با این حال، به دلیل قدرت خورندگی و واکنشپذیری بالا، باید در هنگام کار با آن دقت و نکات ایمنی را رعایت کرد. شناخت ویژگیها، کاربردها و خطرات اسید سولفوریک (H₂SO₄) به ما کمک میکند تا هم از مزایای آن در صنعت بهره ببریم و هم از آسیبهای احتمالی آن به محیط زیست جلوگیری کنیم.
سوالات متداول درباره اسید سولفوریک
۱. اسید سولفوریک چیست و از چه موادی تشکیل شده است؟
اسید سولفوریک یک اسید معدنی بسیار قوی با فرمول شیمیایی H₂SO₄ است که از ترکیب گوگرد، اکسیژن و هیدروژن تشکیل میشود.
۲. مهمترین کاربرد اسید سولفوریک در صنعت چیست؟
بیش از نیمی از تولید جهانی اسید سولفوریک در ساخت کودهای شیمیایی مانند سوپر فسفاتها و آمونیوم فسفات استفاده میشود.
۳. آیا اسید سولفوریک برای انسان خطرناک است؟
بله، تماس مستقیم با این اسید باعث سوختگی پوست و چشم میشود و استنشاق بخارات آن میتواند به دستگاه تنفسی آسیب برساند.
۴. چگونه اسید سولفوریک تولید میشود؟
رایجترین روش تولید آن فرآیند تماسی (Contact Process) است که در آن گوگرد یا سولفیدهای فلزی سوزانده شده و از گازهای حاصل، اسید تولید میشود.
۵. چگونه میتوان اثرات زیستمحیطی اسید سولفوریک را کاهش داد؟
با استفاده از سیستمهای تصفیه گاز، بازیافت اسید مصرفشده، و کنترل نشت در صنایع میتوان آسیبهای زیستمحیطی را به حداقل رساند.

